Scandium (Sc), kémiai elem, a periódusos rendszer 3. csoportjába tartozó ritkaföldfémek.
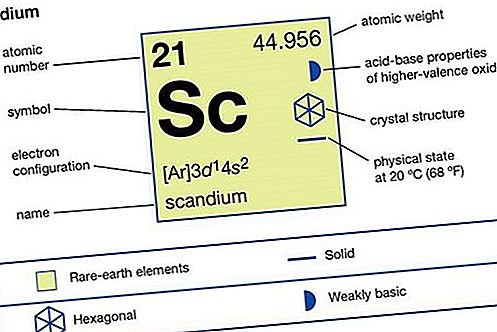
A Scandium ezüstfehér, mérsékelten lágy fém. Meglehetősen stabil a levegőben, de lassan megváltoztatja színét ezüstfehérről sárgás színűre, mert a felületen Sc 2 O 3 -oxid képződik. A fém lassan oldódik hígított savakban - kivéve a hidrogén-fluoridot (HF), amelyben egy védő trifluorid réteg megakadályozza a további reakciót. A skandium paramagnetikus 0 K (–273 ° C vagy –460 ° F) hőmérséklettől olvadáspontjáig (1,541 ° C vagy 2,806 ° F). 186 kilobart meghaladó nyomáson -273,1 ° C (-459,6 ° F) hőmérsékleten szupravezetővé válik.
Miután Dmitrij Ivanovics Mendelejev 1871-ben az orosz kémikus előre jelezte ennek az elemnek a létezését, kezdetben ekaboronnak nevezve, Lars Fredrik Nilson svéd kémikus 1879-ben 1879-ben felfedezte oxidját, a skandiat a ritkaföldfémekben található gadolinitban és euxenitben, míg a svéd vegyész Per Teodor Cleve később, 1879-ben. a skandiumot hipotetikus ekaboronként azonosította. A szandént kis arányban, általában kevesebb, mint 0,2 százalékban találják meg számos nehéz lantanidérc, sok ón-, urán- és volfrámérc esetében. A Thortveitite (szkandium-szilikát) az egyetlen ásványi anyag, amely nagy mennyiségben, kb. 34 százalékban tartalmaz szkandiumot, de sajnos ez az ásvány meglehetősen ritka, és nem fontos szkandiumforrás. A skandium kozmikus előfordulása viszonylag magas. Bár ez csak a Föld 50. leggazdagabb elemét képezi (bősége hasonló a berilliuméhoz), a Nap 23. legszélesebb körű eleme.
A természetben a szandium egy stabil izotóp, a szkandium-45 formájában létezik. A 25 (a nukleáris izomereket kivéve) 36–61 tömegű radioaktív izotóp közül a legstabilabb a szandium-46 (felezési ideje 83,79 nap), és a legkevésbé stabil a szandium-39 (felezési ideje kevesebb, mint 300 nanosekundum).).
A Scandiumot a többi ritkaföldfémből elválasztják az oldhatatlan kálium-szandium-szulfát kicsapása vagy a szandium-tiocianát dietil-éterrel történő extrahálása útján. Maga a fémet először 1938-ban állították elő kálium-, lítium- és szandium-kloridok elektrolízisével eutektikus keverékben (azaz olyan keverékben, amelynek az olvadáspontja a lehető legalacsonyabb ezen komponensekkel). A Scandiumot jelenleg elsősorban uránnal történő extrakció melléktermékeként állítják elő az ásványi daviditből, amely körülbelül 0,02% szandium-oxidot tartalmaz. A Scandium két allotrop (strukturális) formában létezik. Az α-fázis szorosan hatszögletű, a = 3,3088 Å és c = 5,2680 Å szobahőmérsékleten. A β-fázis testközpontú köbméter, becsült a = 3,73 Å, 1337 ° C (2,439 ° F) hőmérsékleten.
Ennek a szokatlan átmeneti fémnek csak néhány felhasználását fejlesztették ki, elsősorban a skandium korlátozott elérhetősége és magas költségei miatt. Kis sűrűsége és magas olvadáspontja ötvözőszerként szolgál könnyűfémek katonai és nagy teljesítményű alkalmazásokhoz. A skandium legfontosabb felhasználása az alumínium alapú ötvözetek ötvözete a sportcikkekben és a nagy intenzitású fémhalogenid lámpákban. Alumíniummal és alumínium alapú ötvözetekkel ötvözve a skandium korlátozza a magas hőmérsékleten történő gabona növekedését.
A skandium kémiája jobban hasonlít a többi oxidációs állapot ritkaföldfémeinek eleméhez, mint az alumínium vagy a titánéhoz. Néhány viselkedése azonban atipikus a ritkaföldfémektől, mert lényegesen kisebb ion sugara (1,66 Å a 12. koordinációs számnál), összehasonlítva a ritkaföldfémek átlagával (1,82 Å a 12. koordinációs számmal). Emiatt az Sc 3+ ion egy viszonylag erős sav, és sokkal nagyobb hajlammal bonyolult ionokat képez.
Az elem tulajdonságai
| atomszám | 21 |
|---|---|
| atomtömeg | 44,95591 |
| olvadáspont | 1,541 ° C (2,806 ° F) |
| forráspont | 2836 ° C (5137 ° F) |
| fajsúly | 2,989 (24 ° C vagy 75 ° F) |
| oxidációs állapot | 3 |
| elektronkonfiguráció | [Ar] 3d 1 4s 2 |