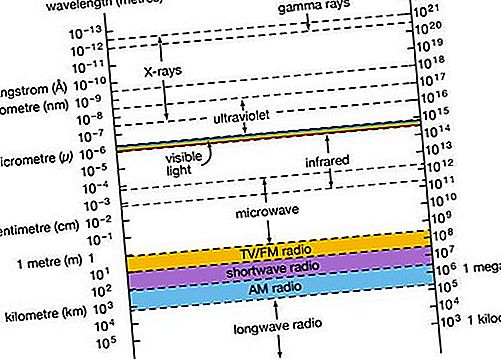
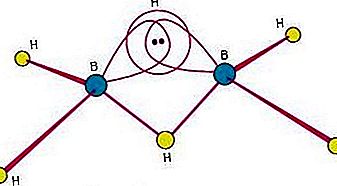
Magnézium-feldolgozás, magnéziumérc előállítása különféle termékekben való felhasználásra.

A magnézium (Mg) ezüstös fehér fém, amely megjelenésében hasonló az alumíniumhoz, ám egyharmadával kevesebb súlyt tartalmaz. Csak 1,738 gramm / köbcentiméter sűrűséggel ez az ismert legkönnyebb szerkezeti fém. Hatszögletű, tömör (hcp) kristályszerkezettel rendelkezik, tehát, mint az ennek a szerkezetnek a legtöbb féme, alacsonyabb hőmérsékleten végzett munka során is hiányzik a rugalmassága. Ezenkívül tiszta formájában a legtöbb szerkezeti alkalmazáshoz elegendő szilárdságú. Az ötvözőelemek hozzáadása azonban olyan mértékben javítja tulajdonságait, hogy mind az öntött, mind a megmunkált magnéziumötvözeteket széles körben használják, különösen ott, ahol a könnyű és nagy szilárdság fontos.
A magnézium magas hőmérsékleten erősen reagál oxigénnel; 645 ° C feletti hőmérsékleten, száraz levegőn, erős fehér fénnyel és erős hővel ég. Ezért magnéziumport használnak a pirotechnikában. Szobahőmérsékleten vízben nem oldódó magnézium-hidroxid stabil film képződik a fém felületén, védve a korrózió ellen a legtöbb légkörben. Mivel a magnézium erős reagálószer, amely stabil vegyületeket képez klórral, oxigénnel és kénnel, a magnéziumnak számos fémmegmunkálási felhasználása van, például titán előállításánál titán-tetrakloridból és az olvasztókemence kéntelenítésében. Kémiai reakcióképessége nyilvánvaló azokban a magnéziumvegyületekben is, amelyek széles körben alkalmazhatók az iparban, az orvostudományban és a mezőgazdaságban.
Történelem
A magnézium a magnezitből, egy magnézium-karbonát ásványból származik, és állítólag ez az ásvány tartozik a magnezit lerakódásoknak, amelyek Magánszékben találhatók, egy régi részben Thesszália ókori görög régiójában. Humphry Davy brit kémikus állítólag 1808-ban magnézium-amalgámot állított elő nedves magnézium-szulfát elektrolizálásával, higanyt használva katódként. Az első fém magnéziumot azonban 1828-ban az A.-A.-B francia tudós gyártotta. Elfoglalt. Munkája az olvadt magnézium-klorid fémes káliummal történő redukciója volt. 1833-ban Michael Faraday angol tudós készítette először az magnéziumot az olvadt magnézium-klorid elektrolízisével. Kísérleteit Robert Bunsen német vegyész megismételte.
Az első sikeres ipari termelést Németországban 1886-ban kezdte meg az Aluminium und Magnesiumfabrik Hemelingen, az olvadt karnallit elektrolízise alapján. A Hemelingen később az IG Farbenindustrie ipari komplexum részévé vált, amely az 1920-as és a 30-as évek során nagy mennyiségű olvadt és lényegében vízmentes magnézium-klorid előállítására szolgáló eljárást fejlesztett ki (ma IG Farben eljárás néven ismert), valamint a technológiát. a termék magnézium-fém és klór elektrolizálására. Az IG Farben további hozzájárulása volt számos öntött és alakítható ötvözet, finomító és védőáramok, megmunkált magnéziumtermékek, valamint számos repülőgép- és gépjármű-alkalmazás fejlesztése. A második világháború alatt az Egyesült Államok Dow Chemical Company és az Egyesült Királyság Magnesium Elektron Limited elindította a magnézium elektrolitikus redukcióját a texasi Galveston-öbölből és az Északi-tengertől szivattyúzott tengervízből, az angliai Hartlepoolban. Ugyanakkor a kanadai Ontario-ban bevezették az LM Pidgeon folyamatát, amely szerint a magnézium-oxidot szilíciummal hősen redukálják a külső tüzelésű utómunkákban.
A háborút követően a katonai alkalmazások kiemelt jelentőséggel bírtak. A Dow Chemical kibővítette a polgári piacokat kovácsolt termékek, fotógravírozási technológia és felületkezelő rendszerek fejlesztésével. Az extrakció továbbra is az elektrolízis és a hőcsökkentés alapja. Ezekre a folyamatokra olyan finomításokat hajtottak végre, mint a retúrák belső melegítése (a Magnetherm eljárás, amelyet Franciaországban vezettek be 1961-ben), extrahálás dehidratált magnézium-klorid-pirulákból (a norvég Norsk Hydro társaság vezette be 1974-ben) és az elektrolitikus cellás technológia fejlesztése a 1970 körül.
2019-ig Kína a világ magnéziumának körülbelül 85% -át, míg a fennmaradó rész Oroszország, Kazahsztán, Izrael és Brazília termelte.
Ércek és alapanyagok
A természet nyolcadik legszélesebb eleme, a magnézium a Föld kéregének 2,4% -a. Erős reakcióképessége miatt nem fordul elő natív állapotban, hanem sokféle vegyületben megtalálható a tengervízben, sós lében és kőzetekben.
Az érc ásványi anyagok közül a legelterjedtebbek a karbonátok (dolomit) (magnézium- és kalcium-karbonátok vegyülete, MgCO 3 · CaCO 3) és a magnezit (magnézium-karbonát, MgCO 3). Kevésbé gyakori a hidroxid ásványi brucit, Mg (OH) 2 és a halogenid ásványi karnallit (magnézium- és kálium-kloridok és víz vegyülete, MgCl 2 · KCl · 6H 2 O).
A magnézium-klorid visszatéríthető a természetben előforduló sós sókból, például a Nagy Sós-tóból (amely jellemzően 1,1 tömegszázalék magnéziumot tartalmaz) és a Holt-tengertől (3,4 százalék), ám messze a legnagyobb forrás a világ óceánjai. Bár a tengervíz csak körülbelül 0,13% magnéziumot tartalmaz, szinte kimeríthetetlen forrást jelent.
Bányászat és koncentrálás
A dolomitot és a magnezitet is szokásos módszerekkel bányászják és koncentrálják. A karnallitot ércként ásatják, vagy elválasztják más sóvegyületektől, amelyeket az oldatbányászat a felszínre hoz. A természetben előforduló magnéziumtartalmú sós sókat nagy tókon koncentrálják napfény elpárologtatással.
Kitermelés és finomítás
Erős kémiai reagens, a magnézium stabil vegyületeket képez és oxigénnel és klórral reagál mind folyékony, mind gáznemű állapotban. Ez azt jelenti, hogy a fém nyersanyagokból történő extrahálása energiaigényes folyamat, amely jól hangolt technológiákat igényel. A kereskedelmi termelés két teljesen eltérő módszert követ: a magnézium-klorid elektrolízisét vagy a magnézium-oxid termikus redukcióját a Pidgeon-eljáráson keresztül. Az elektrolízis a világ magnéziumtermelésének körülbelül 75% -át tette ki. A 21. század elején azonban, amikor Kína lett a világ vezető magnéziumtermelője, az ott levő alacsony munkaerő és energia költségek lehetővé tették a Pidgeon-folyamat gazdasági életképességét annak ellenére, hogy kevésbé hatékony, mint az elektrolízis.
Elektrolízis
Az elektrolitikus folyamatok két lépésből állnak: magnézium-kloridot tartalmazó alapanyag előállítása és ennek a vegyületnek az elektrolitikus cellákban magnézium-fémré és klórgázzá történő disszociálása.
Az ipari folyamatokban a sejttakarmányok különféle olvadt sókból állnak, amelyek vízmentes (lényegében vízmentes) magnézium-kloridot, részlegesen dehidratált magnézium-kloridot vagy vízmentes karnallitot tartalmaznak. A karnallitércek szennyeződéseinek elkerülése érdekében a dehidrált mesterséges karnallitot szabályozott kristályosítással állítják elő melegített magnézium- és káliumtartalmú oldatokból. Részben dehidrált magnézium-kloridot nyerhetünk a Dow-eljárással, amelynek során a tengervizet flokkulátorban elegyítjük enyhén égett reaktív dolomittal. Egy oldhatatlan magnézium-hidroxid kicsapódik az ülepítő tartály aljára, majd szuszpenzióként pumpálják, szűrik, sósavval reagáltatva magnézium-kloriddá alakítják, és párologtatási lépések sorozatában szárítják 25% víztartalomra. A végső kiszáradásra az olvasztás során kerül sor.
A vízmentes magnézium-kloridot két fő módszerrel állítják elő: a magnézium-klorid-sóoldatok víztelenítésével vagy a magnézium-oxid klórozásával. Az utóbbi módszernél, amelyet az IG Farben eljárással szemléltetünk, az enyhén égett dolomitot tengervízzel keverjük össze egy flokkulátorban, ahol magnézium-hidroxid kicsapódik, leszűrjük és magnézium-oxiddá kalcináljuk. Ezt összekeverjük faszénnel, gömbökké alakítjuk magnézium-klorid-oldat hozzáadásával és megszárítjuk. A gömböcskéket egy klórozóba, egy téglával bélelt tengelyes kemencébe töltik, ahol szénelektródákkal körülbelül 1000–1200 ° C-ra hevítik őket (1800–2200 ° F). A kemencében lévő nyílásokon keresztül bejutott klórgáz reakcióba lép a magnézium-oxiddal, így megolvadt magnézium-klorid képződik, amelyet időközönként megcsapolnak és továbbítanak az elektrolitikus cellákba.
A magnézium-sóoldatok dehidrálását szakaszosan végzik. A Norsk Hydro eljárás során a szennyeződéseket először kicsapással és szűréssel távolítják el. A tisztított sóoldatot, amely körülbelül 8,5% magnéziumot tartalmaz, betöményítéssel 14% -ra koncentrálják, és részecskékké alakítják át a töltőtoronyban. Ezt a terméket vízmentes részecskékké szárítják, és továbbítják az elektrolitikus cellákba.
Az elektrolitikus cellák lényegében téglával bélelt edények, amelyek több acél katóddal és grafit anóddal vannak felszerelve. Ezeket függőlegesen a cellafedélre szerelik fel, és részlegesen merítik egy lúgos kloridokból álló olvadt sóelektrolitba, amelyhez a fent leírt eljárások során előállított magnézium-kloridot 6-18% koncentrációban adják hozzá. Az alapvető reakció:
Az üzemi hőmérséklet 680-750 ° C (1,260-1,380 ° F). Az energiafogyasztás 12-18 kilowattóra / kg előállított magnézium. Klórt és más gázokat állítanak elő a grafit anódokon, és az olvadt magnézium-fém lebeg a sófürdő tetejére, ahol összegyűjtik. A klór újra felhasználható a dehidratációs folyamatban.
Hőcsökkentés
A hőtermelés során a dolomitot magnézium-oxiddá (MgO) és mészké (CaO) kalcinálják, ezeket szilíciummal (Si) redukálják, magnéziumgázt és salak dikalcium-szilikátot kapva. Az alapvető reakció, endotermikus, vagyis hőt kell alkalmazni annak elindításához és fenntartásához. Ha a magnézium eléri a 100 kilopascal (1 atmoszféra) gőznyomást 1800 ° C (3270 ° F) hőmérsékleten, a hőigény elég magas lehet. A reakcióhőmérséklet csökkentése érdekében az ipari folyamatok vákuumban működnek. Három fő módszer létezik, amelyek a hőellátásuk szempontjából különböznek egymástól. A Pidgeon-folyamat során az őrölt és kalcinált dolomitot finoman őrölt ferroszilíciummal keverik össze, brikettálják és hengeres nikkel-króm-acél retrótokba töltik. Számos retró vízszintesen van beépítve egy olaj- vagy gáztüzelésű kemencébe, fedőikkel és csatolt kondenzátorrendszereikkel a kemencéből kinyúlva. Az 1200 ° C (2,200 ° F) hőmérsékleten és 13 paszál csökkentett nyomáson végzett reakcióciklus után a kondenzátorokból magnéziumkristályokat (úgynevezett koronákat) távolítanak el, a salakot szilárd anyagként evakuálják, és a retortát újratöltik. A Bolzano-folyamat során a dolomit-ferroszilícium-brikettet egy speciális töltőtámasz-rendszerre rakják, amelyen keresztül a belső elektromos fűtés vezet a töltéshez. A teljes reakció 20–24 órát vesz igénybe 1200 ° C hőmérsékleten, 400 pasztila mellett.
A fenti eljárásokkal előállított dikalcium-szilikát salak olvadáspontja körülbelül 2000 ° C (3 600 ° F), és ezért szilárd anyag formájában van jelen, de az alumínium-oxid (alumínium-oxid, Al 2 O 3) hozzáadásakor a Az olvadáspont 1550–1 600 ° C-ra (2 825–2 900 ° F) csökkenthető. Ennek a Magnetherm eljárásban alkalmazott módszernek az az előnye, hogy a folyékony salak közvetlenül vízmelegítéssel, vízhűtéses réz-elektródon keresztül elektromos árammal melegíthető. A redukciós reakció 1600 ° C-on és 400–670 paszkál nyomáson megy végbe. A párologtatott magnéziumot a reaktorhoz kapcsolódó külön rendszerben kondenzálják, és az olvadt salakot és a ferroszilíciumot időközönként megcsapolják.